Tvärbindning

Vid tvärbindning binds polymerer, molekylkedjor, ihop till tredimensionella nätverk, med kovalenta bindningar eller jonbindningar[1] och polymererna kan vara antingen syntetiska polymerer eller naturliga polymerer (såsom proteiner). Man talar här även om "förnätning".

Det är en form av härdning, där det tvärbundna ämnet får ökad hållbarhet. Ett exempel på detta är härdplast, som efter härdning inte längre är smältbart, på grund av tvärbindningarna i materialet.
När "tvärbindning" används inom det biologiska området, hänvisar det till användningen av en sond för att länka samman proteiner för att kontrollera protein-protein-interaktioner, såväl som andra kreativa tvärbindningsmetoder. Även om termen används för att hänvisa till "bindning av polymerkedjor" för båda vetenskaperna, varierar graden av tvärbindning och specificiteterna för tvärbindningsmedlen mycket.
Syntetiska polymerer
[redigera | redigera wikitext]
Kemiska reaktioner förknippade med tvärbindning av torkande oljor, processen som producerar linoleum.
Tvärbindning inhåller i allmänhet kovalenta bindningar som förenar två polymerkedjor. Termen härdning hänvisar till tvärbindning av härdplaster, som omättad polyester och epoxiharts och termen vulkanisering används typiskt för gummin.[2] När polymerkedjor tvärbinds blir materialet styvare. De mekaniska egenskaperna hos en polymer beror starkt på tvärbindningsdensiteten. Låga tvärbindningsdensiteter ökar polymersmältornas viskositet. Mellanliggande tvärbindningsdensiteter omvandlar gummiartade polymerer till material som har elastomera egenskaper och potentiellt höga hållfastheter. Mycket höga tvärbindningsdensiteter kan göra att material blir mycket styva eller glasiga, som fenol-formaldehydmaterial.[3]

Vid användning behandlas opolymeriserat eller delvis polymeriserat harts med ett tvärbindningsreagens. Vid vulkanisering är svavel tvärbindningsmedlet. Dess introduktion ändrar gummi till ett styvare, hållbart material till exempel bil- och cykeldäck. Denna process kallas ofta svavelhärdning. I de flesta fall är tvärbindning irreversibel, och det resulterande värmehärdande materialet kommer att brytas ned eller brinna om det upphettas utan att smälta. Kemiska kovalenta tvärbindningar är stabila mekaniskt och termiskt. Därför kan tvärbundna produkter som bildäck inte lätt återvinnas.
En klass av polymerer känd som termoplastiska elastomerer förlitar sig på fysiska tvärbindningar i dess mikrostruktur för att uppnå stabilitet, och används i stor utsträckning i icke-däcktillämpningar, som snöskoterbanor och katetrar för medicinskt bruk. De erbjuder ett mycket bredare spektrum av egenskaper än konventionella tvärbundna elastomerer eftersom de domäner som fungerar som tvärbindningar är reversibla, så att de kan omvandlas genom värme. De stabiliserande domänerna kan vara icke-kristallina (som i styren-butadien-segmentsampolymerer) eller kristallina som i termoplastiska sampolyestrar.

Alkydemaljer, den dominerande typen av kommersiell oljebaserad färg, härdar genom oxidativ tvärbindning efter exponering för luft.[5]
Fysiska tvärbindningar
[redigera | redigera wikitext]I motsats till kemiska tvärbindningar bildas fysikaliska tvärbindningar av svagare interaktioner. Till exempel natriumalginatgeler vid exponering för kalciumjoner, som bildar jonbindningar som överbryggar alginatkedjor.[6] Polyvinylalkoholgeler vid tillsats av borax genom vätebindning mellan borsyra och polymerens alkoholgrupper.[7][8] Andra exempel på material som bildar fysiskt tvärbundna geler är gelatin, kollagen, agaros och agar-agar.
Mätning av tvärbindingsgrad
[redigera | redigera wikitext]Tvärbindning mäts ofta med svällningstester. Det tvärbundna provet placeras i ett bra lösningsmedel vid en specifik temperatur, och antingen ändringen i massa eller ändringen i volym mäts. Ju mer tvärbindning, desto mindre svällning kan uppnås. Baserat på graden av svällning, Florys interaktionsparameter (som relaterar lösningsmedelsinteraktionen med provet) och lösningsmedlets densitet, kan den teoretiska tvärbindningsgraden beräknas enligt Florys nätverksteori.[9]
Två ASTM-standarder används vanligtvis för att beskriva graden av tvärbindning i termoplaster. I ASTM D2765 vägs provet, placeras sedan i ett lösningsmedel under 24 timmar, vägs igen medan det är svällt, torkas sedan och vägs en sista gång.[10] Graden av svällning och den lösliga delen kan beräknas. I en annan ASTM-standard, F2214, placeras provet i ett instrument som mäter höjdförändringen i provet, vilket gör att användaren kan mäta volymförändringen.[11] Tvärbindningsdensiteten kan sedan beräknas.
I biologi
[redigera | redigera wikitext]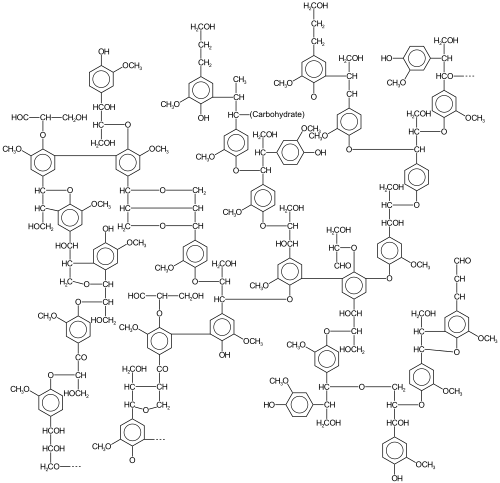
Lignin
[redigera | redigera wikitext]Lignin är en starkt tvärbunden polymer som utgör det huvudsakliga strukturella materialet i högre växter. Ett hydrofobt material, det härrör från prekursormonolignoler. Heterogenitet uppstår från mångfalden och graden av tvärbindning mellan dessa lignoler.
I DNA
[redigera | redigera wikitext]
Intrasträngad DNA-tvärbindning har starka effekter på organismer eftersom dessa lesioner stör transkription och replikation. Dessa effekter kan användas på ett bra sätt (mot cancer) eller så kan de vara dödliga för värdorganismen. Läkemedlet cisplatin fungerar genom bildning av intrasträngtvärbindningar i DNA.[12] Andra tvärbindningsmedel är senapsgas, mitomycin och psoralen.[13]
Proteiner
[redigera | redigera wikitext]I proteiner är tvärbindningar viktiga för att generera mekaniskt stabila strukturer som hår och ull, hud och brosk. Disulfidbindningar är vanliga tvärbindningar.[14] Bildning av isopeptidbindningar är en annan typ av proteintvärbindning. Processen att applicera en permanent våg i hår involverar brytning och reformering av disulfidbindningar. Typiskt används en merkaptan såsom ammoniumtioglykolat för brytningen. Efter detta krullas håret och "neutraliseras" sedan. Neutralisatorn är vanligtvis en sur lösning av väteperoxid, som gör att nya disulfidbindningar bildas, vilket permanent fixerar håret till sin nya konfiguration. Komprometterat kollagen i hornhinnan, ett tillstånd som kallas keratokonus, kan behandlas med klinisk tvärbindning.[15] I biologiska sammanhang kan tvärbindning spela en roll vid åderförkalkning genom avancerad glykeringsslutprodukter (AGEer), som har medverkat till att inducera tvärbindning av kollagen, vilket kan leda till vaskulär stelning.[16]
Forskning
[redigera | redigera wikitext]Proteiner kan också tvärbindas artificiellt med användning av småmolekylära tvärbindare. Detta tillvägagångssätt har använts för att belysa protein-protein-interaktioner.[17][18][19] Tvärbindare binder endast ytrester i relativt nära närhet i det naturliga tillståndet. Vanliga tvärbindare inkluderar imidoestertvärbindaren dimetylsuberimidat, N-hydroxisuccinimid-estertvärbindaren BS3 och formaldehyd. Var och en av dessa tvärbindare inducerar nukleofil attack av aminogruppen av lysin och efterföljande kovalent bindning via tvärbindaren. Karbodiimidtvärbindaren EDC med noll längd fungerar genom att omvandla karboxyler till aminreaktiva isourea-mellanprodukter som binder till lysinrester eller andra tillgängliga primära aminer. SMCC eller dess vattenlösliga analog, Sulfo-SMCC, används vanligtvis för att framställa antikropphaptenkonjugat för antikroppsutveckling. En in vitro tvärbindningsmetod är PICUP (fotoinducerad tvärbindning av omodifierade proteiner).[20] Typiska reagenser är ammoniumpersulfat (APS), en elektronacceptor, fotosensibilisatorn tris-bipyridylrutenium (II) katjon ([Ru(bpy)3] 2+).[20] I in vivo tvärbindning av proteinkomplex odlas celler med fotoreaktiva diazirinanaloger till leucin och metionin, som är inkorporerade i proteiner. Vid exponering för ultraviolett ljus aktiveras diazirinerna och binder till interagerande proteiner som finns inom några få ångströms av den fotoreaktiva aminosyraanalogen (UV-tvärbindning).[21]
Se även
[redigera | redigera wikitext]Referenser
[redigera | redigera wikitext]- Den här artikeln är helt eller delvis baserad på material från engelskspråkiga Wikipedia, 27 juli 2024.
Noter
[redigera | redigera wikitext]- ^ Polymers Arkiverad 2 oktober 2015 hämtat från the Wayback Machine. Pennsylvania State University, Department of Chemistry. Läst 1 november 2017.
- ^ Hans Zweifel; Ralph D. Maier; Michael Schiller (2009). Plastics additives handbook (6th). Munich: Hanser. Sid. 746. ISBN 978-3-446-40801-2.
- ^ Gent, Alan N. (1 April 2018). Engineering with Rubber: How to Design Rubber Components. Hanser. ISBN 9781569902998. https://books.google.com/books?id=q034u2kLAagC&pg=PA22. Läst 1 april 2018.
- ^ Pham, Ha Q.; Marks, Maurice J. (2012). ”Epoxy Resins”. Ullmann's Encyclopedia of Industrial Chemistry. doi:. ISBN 978-3527306732.
- ^ Abraham, T.W.; Höfer, R. (2012), ”Lipid-Based Polymer Building Blocks and Polymers” (på engelska), Polymer Science: A Comprehensive Reference (Elsevier): s. 15–58, doi:, ISBN 978-0-08-087862-1, https://linkinghub.elsevier.com/retrieve/pii/B9780444533494002533, läst 27 juni 2022
- ^ Hecht, Hadas; Srebnik, Simcha (2016). ”Structural Characterization of Sodium Alginate and Calcium Alginate”. Biomacromolecules 17 (6): sid. 2160–2167. doi:. PMID 27177209.
- ^ ”Experiments: PVA polymer slime”. Education: Inspiring your teaching and learning. Royal Society of Chemistry. 2016. https://edu.rsc.org/experiments/pva-polymer-slime/756.article. ”A solution of polyvinyl alcohol (PVA) can be made into a slime by adding borax solution, which creates cross-links between polymer chains.”
- ^ Casassa, E.Z; Sarquis, A.M; Van Dyke, C.H (1986). ”The gelation of polyvinyl alcohol with borax: A novel class participation experiment involving the preparation and properties of a "slime"”. Journal of Chemical Education 63 (1): sid. 57. doi:. Bibcode: 1986JChEd..63...57C.
- ^ Flory, P.J., "Principles of Polymer Chemistry" (1953)
- ^ ”ASTM D2765 - 16 Standard Test Methods for Determination of Gel Content and Swell Ratio of Crosslinked Ethylene Plastics”. www.astm.org. http://www.astm.org/Standards/D2765.htm.
- ^ ”ASTM F2214 - 16 Standard Test Method for In Situ Determination of Network Parameters of Crosslinked Ultra High Molecular Weight Polyethylene (UHMWPE)”. www.astm.org. http://www.astm.org/Standards/F2214.htm.
- ^ Siddik, Zahid H. (2003). ”Cisplatin: Mode of cytotoxic action and molecular basis of resistance”. Oncogene 22 (47): sid. 7265–7279. doi:. PMID 14576837.
- ^ Noll, David M.; Mason, Tracey Mcgregor; Miller, Paul S. (2006). ”Formation and Repair of Interstrand Cross-Links in DNA”. Chemical Reviews 106 (2): sid. 277–301. doi:. PMID 16464006.
- ^ Christoe, John R.; Denning, Ron J.; Evans, David J.; Huson, Mickey G.; Jones, Leslie N.; Lamb, Peter R.; Millington, Keith R.; Phillips, David G.; et al. (2005). ”Wool”. Kirk-Othmer Encyclopedia of Chemical Technology. doi:. ISBN 9780471484943.
- ^ Wollensak G, Spoerl E, Seiler T. Riboflavin/ultraviolet-a-induced collagen crosslinking for the treatment of keratoconus. Am J Ophthalmol. 2003 May;135(5):620-7.
- ^ Prasad, Anand; Bekker, Peter; Tsimikas, Sotirios (2012-08-01). ”Advanced glycation end products and diabetic cardiovascular disease”. Cardiology in Review 20 (4): sid. 177–183. doi:. ISSN 1538-4683. PMID 22314141.
- ^ ”Pierce Protein Biology - Thermo Fisher Scientific”. www.piercenet.com. http://www.piercenet.com/Objects/View.cfm?type=Page&ID=FE7F690D-58AE-4342-AE85-BA94DCA642F8.
- ^ Kou Qin; Chunmin Dong; Guangyu Wu; Nevin A Lambert (August 2011). ”Inactive-state preassembly of Gq-coupled receptors and Gq heterotrimers”. Nature Chemical Biology 7 (11): sid. 740–747. doi:. PMID 21873996.
- ^ Mizsei, Réka; Li, Xiaolong; Chen, Wan-Na; Szabo, Monika; Wang, Jia-huai; Wagner, Gerhard; Reinherz, Ellis L.; Mallis, Robert J. (January 2021). ”A general chemical crosslinking strategy for structural analyses of weakly interacting proteins applied to preTCR-pMHC complexes”. Journal of Biological Chemistry 296: sid. 100255. doi:. ISSN 0021-9258. PMID 33837736.
- ^ [a b] Fancy, David A.; Kodadek, Thomas (1999-05-25). ”Chemistry for the analysis of protein–protein interactions: Rapid and efficient cross-linking triggered by long wavelength light” (på engelska). Proceedings of the National Academy of Sciences 96 (11): sid. 6020–6024. doi:. ISSN 0027-8424. PMID 10339534. Bibcode: 1999PNAS...96.6020F.
- ^ Suchanek, Monika; Anna Radzikowska; Christoph Thiele (April 2005). ”Photo-leucine and photo-methionine allow identification of protein–protein interactions in living cells”. Nature Methods 2 (4): sid. 261–268. doi:. PMID 15782218.

