Diol

Dioler är organisk-kemiska föreningar som innehåller två hydroxigrupper (-OH-grupper).[1] En alifatisk diol kallas också en glykol.[2] Detta kan jämföras med de enkla alkoholer, som till exempel etanol, som bara har en hydroxigrupp. På motsvarande sätt är trioler föreningar som innehåller tre hydroxigrupper.
Den vanligaste industriella diolen är etylenglykol. Exempel på dioler där hydroxylfunktionella grupper är mer åtskilda inkluderar 1,4-Butandiol HO−(CH2)4−OH och propylen-1,3-diol eller betapropylenglykol, HO−CH−CH2−CH2−CH2−CH|||.
Framställning
[redigera | redigera wikitext]Geminala dioler
[redigera | redigera wikitext]En geminal diol har två hydroxylgrupper bundna till samma atom. Dessa arter uppstår genom hydrering av karbonylföreningarna. Hydreringen är vanligtvis ogynnsam, men ett anmärkningsvärt undantag är formaldehyd som i vatten existerar i jämvikt med metandiol, H2C(OH)2. Ett annat exempel är (F3C)2C(OH)2, den hydratiserade formen av hexafluoraceton. Många geminala dioler genomgår ytterligare kondensation för att ge dimeriska och oligomera derivat. Denna reaktion gäller glyoxal och relaterade aldehyder.
Vicinala dioler
[redigera | redigera wikitext]I en vicinal diol upptar de två hydroxylgrupperna vicinala positioner, det vill säga de är fästa vid intilliggande atomer. Dessa föreningar kallas glykoler. Exempel är etan-1,2-diol eller etylenglykol HO−(CH2)2−OH, en vanlig ingrediens i frostskyddsprodukter. Ett annat exempel är propan-1,2-diol eller alfapropylenglykol, HO−CH−CH2−CH(OH)−CH3, som används inom livsmedels- och medicinindustrin, samt en relativt giftfri frostskyddsprodukt.
I kommersiell skala är huvudvägen till vicinala dioler hydrolys av epoxider. Epoxiderna framställs genom epoxidering av alkenen. Ett exempel är syntesen av transcyklohexanediol[3] eller med mikroreaktor.[4]
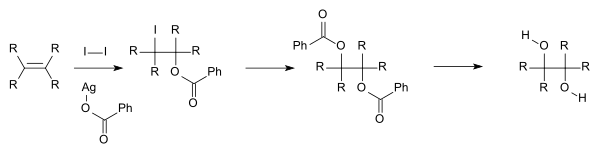
För akademisk forskning och farmaceutiska områden produceras vicinala dioler ofta genom oxidation av alkener, vanligtvis med utspätt surt kaliumpermanganat. Användning av alkaliskt kaliummanganat (VII) ger en färgförändring från klar djuplila till klargrön, medan surt kaliummanganat(VII) blir klart färglöst. Osmiumtetroxid kan på liknande sätt användas för att oxidera alkener till vicinala dioler. Den kemiska reaktionen som kallas Sharpless asymmetrisk dihydroxylering kan användas för att producera kirala dioler från alkener med hjälp av ett osmatereagens och en kiral katalysator. En annan metod är Woodward cis-hydroxylering (cisdiol) och den relaterade Prévostreaktionen (antidiol), avbildad nedan, som båda använder jod och silversaltet av en karboxylsyra.
Andra vägar till vicinala dioler är hydrering av acyloiner[5] och pinacolkopplingsreaktionen.
1,3-dioler
[redigera | redigera wikitext]1,3-dioler framställs ofta industriellt genom aldolkondensation av ketoner med formaldehyd. Den resulterande karbonylen reduceras med användning av Cannizzaroreaktionen eller genom katalytisk hydrering:
- RC(O)CH3 + CH2O → RC(O)CH2CH2OH
- RC(O)CH2CH2OH + H2 → RCH(OH)CH2CH2OH
2,2-Disubstituted propan-1,3-dioler framställs på detta sätt. Exempel är 2-metyl-2-propyl-1,3-propandiol och neopentylglykol.
1,3-dioler kan framställas genom hydrering av α,β-omättade ketoner och aldehyder. Den resulterande ketoalkoholen hydreras. En annan väg är hydroformylering av epoxider följt av hydrering av aldehyden. Denna metod har använts för 1,3-propandiol från etylenoxid.
Mer specialiserade vägar till 1,3-dioler är reaktionen mellan en alken och formaldehyd, Prinsreaktionen. 1,3-dioler kan produceras diastereoselektivt från motsvarande β-hydroxiketoner med hjälp av Evans–Saksena-,Narasaka–Prasad- eller Evans–Tishchenko-reduktionsprotokollen.
1,3-dioler beskrivs som syn eller anti beroende på de relativa stereokemierna hos kolatomerna som bär hydroxylfunktionella grupper. Zinkoforin är en naturlig produkt som innehåller både syn och anti 1,3-dioler.
1,4-, 1,5- och längre dioler
[redigera | redigera wikitext]Dioler där hydroxylgrupperna separeras av flera kolcentra framställs i allmänhet genom hydrering av diestrar av motsvarande dikarboxylsyror:
- (CH2)n(CO2R)2 + 4 H2 → (CH2)n(CH2OH)2 + 2 H2O + 2 ROH
1,4-butandiol,1,5-pentandiol,1,6-hexanediol, 1,10-dekanediol är viktiga råämnen till polyuretaner.[6]
Användning
[redigera | redigera wikitext]Ur det industriella perspektivet är diolernas dominerande reaktioner vid framställning av polyuretaner och alkydhartser.[6]
Dioler som etylenglykol används som sammonomerer i polymerisationsreaktioner som bildar polymerer inklusive vissa polyestrar och polyuretaner. Dioler kan också omvandlas till laktoner genom Fétizon-oxidationsreaktionen.
Se även
[redigera | redigera wikitext]Referenser
[redigera | redigera wikitext]- Den här artikeln är helt eller delvis baserad på material från engelskspråkiga Wikipedia, Diol, 27 oktober 2022.
Noter
[redigera | redigera wikitext]- ^ March, Jerry (1985), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (3rd ed.), New York: Wiley, ISBN 0-471-85472-7.
- ^ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "diols". doi:10.1351/goldbook.D01748..
- ^ trans-cyclohexanediol Organic Syntheses, Coll. Vol. 3, p. 217 (1955); Vol. 28, p.35 (1948) http://www.orgsynth.org/orgsyn/pdfs/CV3P0217.pdf.
- ^ Advantages of Synthesizing trans-1,2-Cyclohexanediol in a Continuous Flow Microreactor over a Standard Glass Apparatus Andreas Hartung, Mark A. Keane, and Arno Kraft J. Org. Chem. 2007, 72, 10235–10238 doi:10.1021/jo701758p.
- ^ Blomquist, A. T.; Goldstein, Albert (1956). ”1,2-Cyclodecanediol”. Organic Syntheses 36: sid. 12. doi:.
- ^ [a b] Peter Werle, Marcus Morawietz, Stefan Lundmark, Kent Sörensen, Esko Karvinen and Juha Lehtonen (2008). "Alcohols, Polyhydric". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a01_305.pub2.
Externa länkar
[redigera | redigera wikitext] Wikimedia Commons har media som rör diol.
Wikimedia Commons har media som rör diol.
|