O-tolidin
| o-tolidin | |
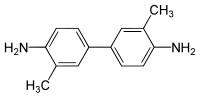 | |
| Systematiskt namn | 4- (4-amino-3-metylfenyl) -2-metylanilin |
|---|---|
| Övriga namn | Ortotolidin; Diaminoditolyl; Diaminotolyl; Bianisidin; Tolidinblått |
| Kemisk formel | C14H16N2 |
| Molmassa | 212,30 g/mol |
| Utseende | Vita till rosa kristaller eller pulver |
| CAS-nummer | 119-93-7 |
| SMILES | CC1=C(C=CC(=C1)C2=CC(=C(C=C2)N)C)N |
| Egenskaper | |
| Densitet | 1,23 g/cm³ |
| Löslighet (vatten) | 1,3 g/l |
| Smältpunkt | 129 °C |
| Kokpunkt | 300,5 °C |
| Faror | |
| Huvudfara | Potentiellt cancerogen |
| SI-enheter & STP används om ej annat angivits | |
o-tolidin (2-tolidin, ortotolidin) är en organisk förening med formeln C14H16N2. Flera isomerer är kända; 3-tolidinderivat är också kommersiellt viktig.
Egenskaper
[redigera | redigera wikitext]o-tolidin är en aromatisk diamin av bifenyltyp. Den är en färglös substans även om varuprover ofta är färgade. Den är något löslig i vatten och bildar salter med syror, såsom hydroklorid, som är kommersiellt tillgänglig.
Framställning
[redigera | redigera wikitext]o-tolidin kan framställas genom en bensidinomlagring från ett hydrazinderivat härlett från 2-nitrotoluen.
- (CH3C6H4)2N2H2 → (C6H3(CH3)NH2)2
Användning
[redigera | redigera wikitext]o-tolidin används kommersiellt främst för framställning av färgämnen. Den har också en funktion för tillverkning av vissa elastomerer. Den är en mellanprodukt för produktion av lösliga azofärgämnen och olösliga pigment som används speciellt inom textil-, läder- och pappersindustrin.
o-tolidin har allmänt användning som en reagens eller indikator i analytisk klinisk och rättskemi, såsom i den analytiska bestämningen av guld, eller bestämning av klornivån i vattenpooler.
Säkerhet
[redigera | redigera wikitext]o-tolidin är giftig och möjligen cancerframkallande. Den är listad som ett IARC grupp 2B cancerframkallande ämne, vilket betyder att den är "möjligen cancerframkallande för människor". Djurstudier har visat att djur exponerade för o-tolidin utvecklade tumörer i lever, njure och mjölkkörtlar.
Hög exponering kan ge irritation i andningsvägarna.
Källor
[redigera | redigera wikitext]- Den här artikeln är helt eller delvis baserad på material från engelskspråkiga Wikipedia, tidigare version.
Externa länkar
[redigera | redigera wikitext]
|
