Arekolin
| Arekolin | |
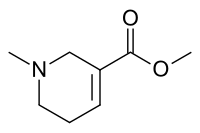  | |
| Systematiskt namn | metyl-1-metyl-1,2,5,6-tetrahydropyridin-3-karboxylat |
|---|---|
| Övriga namn | Arekalin; Arecholine; Arecolin; Arekolin bas; |
| Kemisk formel | C8H13NO2 |
| Molmassa | 155,194 g/mol |
| Utseende | Luktfri vätska |
| CAS-nummer | 63-75-2 |
| SMILES | O=C(OC)C1=CCCN(C)C1 |
| Egenskaper | |
| Densitet | 1,0495 g/cm³ |
| Smältpunkt | 27 °C |
| Kokpunkt | 209 °C |
| SI-enheter & STP används om ej annat angivits | |
Arekolin är en verksam nikotinsyrabaserad mild parasympatomimetisk stimulerande alkaloid i drogen betel, som består arekanöt (betelnöt).[1] Den är en luktfri oljig vätska, som kan ge en känsla av ökad vakenhet och energi, eufori och avkoppling. Dess psykoaktiva effekter är jämförbara med nikotin.
Kemi
[redigera | redigera wikitext]Arekolin är en bas och dess konjugatsyra har en pKa ~ 6,8.[2] Arekolin är flyktigt i ångform, blandbart med de flesta organiska lösningsmedel och vatten, men kan extraheras från vatten med eter i närvaro av upplösta salter. Genom att vara basisk bildar arekolin salter med syror. Salterna är kristallina, men vanligtvis deliquescenta och hydrokloriden, arekolin•HCl, bildar nålar med smältpunkt 158 °C,[2] medan hydrobromiden, arekolin•HBr, bildar smala prismor med smältpunkt 177–179. °C från varm alkohol.
Guldkloriden, arekolin•HAuCl4, är en olja, medan platinikloriden, arekolin2•H2PtCl6, med smältpunkt 176 °C, kristalliserar från vatten i orangeröda romboider. Metodiden bildar blickande prismor med smältpunkt 173-174 °C.
Farmakologi
[redigera | redigera wikitext]Arekolin är den primära aktiva ingrediensen som ansvarar för effekterna av arekanöten i centrala nervsystemet. Arekolin har jämförts med nikotin, som emellertid är antagonist till nikotinacetylkolinreceptorer. Arekolin är däremot främst en partiell agonist av muskarinacetylkolinreceptorer,[3][4] vilket leder till dess parasympatiska effekter.
Hos grodor fungerar arekolin också som en antagonist (eller mycket svag partiell agonist) vid α4- och α6-innehållande nikotinacetylkolinreceptorer och som en tyst antagonist mot α7 nikotinreceptorer; detta kan stå för dess antiinflammatoriska effekter.[5] Arekolin hämmar också AMPK genom generering av ROS i flera typer av celler.[6]
Effekter på nervsystemet
[redigera | redigera wikitext]Arekolin främjar excitation och minskar sömntiden. Det förbättrar också inlärning och minne. Intraperitoneal administrering av arekolin minskar rörelseaktiviteten beroende på intagen dos. Arekolin omvänd skopolamin inducerad minnesförlust. Det kan också minska symtom på depression och schizofreni.[7]
Effekter på hjärt-kärlsystemet
[redigera | redigera wikitext]AN (arekanöt) är en vasodilator främst på grund av närvaron av arekolin. Det har också antitrombos och anti-aterogena effekter genom att öka plasmats kväveoxid, eNos, och mRNA-uttryck och minska IL-8 tillsammans med andra nedregleringar.[7]
Effekter på endokrina systemet
[redigera | redigera wikitext]Arkolin ökar nivån av testosteron genom att stimulera Leydigs celler samt nivåer av FSH och LH.[8][9] Det aktiverar också HPA-axeln och stimulerar CRH-frisättning. Det förhindrar dysfunktion av B-celler i bukspottkörteln från högt fruktosintag.[7]
Effekter på matsmältningssystemet
[redigera | redigera wikitext]Arekolin har förmågan att stimulera matsmältningssystemet genom aktivering av muskarinreceptorer. Extrakt från arekanötvatten kan öka sammandragningarna av magmuskeln och muskelremsor i tolvfingertarmen, ileum, och tjocktarmen avsevärt. Denna aktivitet kan orsakas av arekolin.[7]
Farmakokinetik
[redigera | redigera wikitext]Arekolin metaboliseras av både njurar och lever.[10] För närvarande,är 11 metaboliter av arekolin dokumenterade, bland vilka N-metylnipekotisk syra befunnits vara en viktig metabolit av både arekolin och arekaidin.[11] Kalk sägs hydrolysera nästan alla arekolin till arekaidin, en GABA-återupptagshämmare.[12] Arekaidin bildas också under levermetabolism av arekolin hos råttor.[11]
Användning
[redigera | redigera wikitext]På grund av dess muskariniska och nikotinagonistiska egenskaper, har arekolin visat förbättring av inlärningsförmågan hos friska försökspersoner. Eftersom ett av kännetecknen för Alzheimers sjukdom är en kognitiv nedgång, föreslogs arekolin som en behandling för att sakta ner denna process.
Arekolin administrerat intravenöst har visat en mindre verbal och rumslig minnesförbättring hos Alzheimerpatienter, men på grund av arekolins möjliga cancerframkallande egenskaper[13] är detta inte det första läkemedlet som valts för denna degenerativa sjukdom.[14] I många asiatiska kulturer tuggas arekamuttern tillsammans med betelblad för att få en stimulerande effekt.[15]
Se även
[redigera | redigera wikitext]Referenser
[redigera | redigera wikitext]- Den här artikeln är helt eller delvis baserad på material från engelskspråkiga Wikipedia, Arecoline, 21 augusti 2022.
Noter
[redigera | redigera wikitext]- ^ ”Arecoline M1 receptor activation is a requirement for arecoline analgesia”. Il Farmaco 56 (5–7): sid. 383–5. 2001. doi:. PMID 11482763.
- ^ [a b] The Merck Index, 10th Ed. (1983) p.113, Rahway: Merck & Co.
- ^ ”Differential Receptor Occupancy requirements for Muscarinic Cholinergic Stimulation of Inositol Lipid Hydrolysis in Brain and in Neuroblastomas”. citeseerx.ist.psu.edu. https://citeseerx.ist.psu.edu/messages/downloadsexceeded.html.
- ^ Mei, Lin (1990). ”Pharmacologic Comparison of Selected Agonists for the M1 Muscarinic Receptor in Transfected Murine Fibroblast Cells (B82)”. Pharmacologic Comparison of Selected Agonists for the M1 Muscarinic Receptor in Transfected Murine Fibroblast Cells (B82). https://ia601409.us.archive.org/32/items/Mei-et-al-1990/689.full.pdf.
- ^ Papke, Roger L.; Horenstein, Nicole A.; Stokes, Clare (2015). ”Nicotinic Activity of Arecoline, the Psychoactive Element of "Betel Nuts", Suggests a Basis for Habitual Use and Anti-Inflammatory Activity”. PLOS ONE 10 (10): sid. e0140907. doi:. PMID 26488401. Bibcode: 2015PLoSO..1040907P.
- ^ ”Arecoline-mediated inhibition of AMP-activated protein kinase through reactive oxygen species is required for apoptosis induction”. Oral Oncology 47 (5): sid. 345–51. May 2011. doi:. PMID 21440488.
- ^ [a b c d] Liu, Yu-Jie; Peng, Wei; Hu, Mei-Bian; Xu, Min; Wu, Chun-Jie (2016). ”The pharmacology, toxicology and potential applications of arecoline: A review”. Pharmaceutical Biology 54 (11): sid. 2753–2760. doi:. PMID 27046150.
- ^ Wang, S. W.; Hwang, G. S.; Chen, T. J.; Wang, P. S. (2008). ”Effects of arecoline on testosterone release in rats”. American Journal of Physiology. Endocrinology and Metabolism 295 (2): sid. E497-504. doi:. PMID 18559981. https://pubmed.ncbi.nlm.nih.gov/18559981/.
- ^ Saha, Indraneel; Das, Joydeep; Maiti, Biswaranjan; Chatterji, Urmi (2015). ”A Protective Role of Arecoline Hydrobromide in Experimentally Induced Male Diabetic Rats”. BioMed Research International 2015: sid. 1–12. doi:. PMID 25695047.
- ^ ”Arecoline - an overview | ScienceDirect Topics”. Arecoline - an overview | ScienceDirect Topics. https://www.sciencedirect.com/topics/neuroscience/arecoline.
- ^ [a b] ”A metabolomic approach to the metabolism of the areca nut alkaloids arecoline and arecaidine in the mouse”. Chemical Research in Toxicology 19 (6): sid. 818–27. June 2006. doi:. PMID 16780361.
- ^ Johnston, G. A. R.; Krogsgaard-Larsen, P.; Stephanson, A. (1975). ”Betel nut constituents as inhibitors of γ-aminobutyric acid uptake”. Nature 258 (5536): sid. 627–628. doi:. ISSN 0028-0836. PMID 1207742. Bibcode: 1975Natur.258..627J. https://ui.adsabs.harvard.edu/abs/1975Natur.258..627J/abstract.
- ^ ”Arecoline-induced changes of poly-ADP-ribosylation of cellular proteins and its influence on chromatin organization.”. Cancer Letters 139 (1): sid. 59–65. 1999. doi:. PMID 10408909.
- ^ ”Physostigmine and arecoline: effects of intravenous infusions in Alzheimer's presenile dementia”. British Journal of Psychiatry 138 (1): sid. 46–50. 1981. doi:. PMID 7023592.
- ^ Gupta Prakash Chandra; Ray Cecily S (July 2004). ”Epidemiology of betel quid usage”. Ann. Acad. Med. Singap. 33 (4 Suppl): sid. 31–6. PMID 15389304. http://www.annals.edu.sg/pdf200409/V33N4p31S.pdf.
Externa länkar
[redigera | redigera wikitext] Wikimedia Commons har media som rör Arekolin.
Wikimedia Commons har media som rör Arekolin.
